|
ОСТРЫЙ ЛИМФОБЛАСТНЫЙ ЛЕЙКОЗ
Лейкозы - являются первичным опухолевым заболеванием костного мозга, при котором опухолевые клетки, поражая костный мозг, распространяются не только по органам кроветворения, но и в ЦНС, и в другие органы и системы. Это наиболее частые злокачественные новообразования у детей (частота 1:20000), в возрасте до 4 лет. Согласно современной схеме кровотворения, острые лейкозы объединяет общий признак: субстракт опухоли составляют бластные клетки. При хронических лейкозах субстрактом опухоли являются созревающие и зрелые клетки.
ЭТИОЛОГИЯ.
По имеющимся данным, лейкозы "полиэтиологичны ", т.к. не установлено какой-либо безусловно вызывающей лейкоз причины. Причинными факторами лейкоза человека могут быть химические (экзо- и эндогенные) и физические (ионизирующая радиация) факторы, а также вирусы.
Рауншенбах М.О. с соавт., 1974г., обнаружил у больных лейкозом людей некоторые в-ва из метаболитов триптофана и тирозина, которые способны индуцировать лейкозы и опухоли у мышей.
У человека найден вирус лимфомы Беркитта и выявлена транскриптаза, которая способствует синтезу ДНК на вирусной РНК, что приводит к образованию эндосимбиоза онкогенного вируса и клетки. Это позволило считать обоснованной вирусную этиологию лейкозов.
По гипотезе Р. Хабнера, 1976 г., в геноме каждой клетки заложена информация в виде ДНК-провируса, равноценная информации в геноме онковируса. В норме ДНК-провирус (онкоген) находится в репрессированном состоянии, однако под воздействием концерогенных факторов (химических, радиации) он активизируется и вызывает клеточную трансформацию. Провирус передается по наследству. Некоторые ученые допускают возможность существования систем, подавляющих вирусную лейкозную трансформацию в клетках хозяина, в частности системы, ответственной за иммунитет. Таким образом, в этиологии заболевания главную роль играет не инфицированность вирусом, а состояние контролирующих систем, стимулирующих факторов.
Радиационный этиологический фактор в последние десятилетия привлек внимание как реально существующий фактор внешней среды и внутренней среды человека, способный вызывать лейкоз.
Радиациональные лейкозы человека реально существуют. Это лейкозы у жителей Японии, возникающие много лет спустя после взрывов атомных бомб в Хиросиме и Нагосаки.
Нами была выявлена связь между ростом заболеваемостью лейкозом и загрязнением воздуха некоторыми полютантами воздуха в таких районах Крыма как Сакский, Бахчисарайский, Раздольненский и др.
Итак, этиология лейкозов находится в стадии изучения.
ПАТОГЕНЕЗ.
О патологической сущности лейкозов известно, что лейкоз это опухоль. В основе его лежит первичная патология клеток кроветворения, сопровождающаяся нарушением процессов их пролиферации и дифференцирования, возникновение клонов опухолевых (лейкозных) клеток. Прогрессирующая прлиферация этих клеток приводит к поражению органов кроветворения и уменьшению плацдарма нормального гемопоэза.
Учение о развитии лейкозного процесса, понятие об опухолевой прогрессии при лейкозах ввел А.И. Воробъев в 1965 г. В настоящее время это учение разработано применительно ко всем формам лейкоза с соответствующими патогенетическими мероприятиями терапии.
Бластные клетки при остром лейкозе теряют ферментную специфичность. Клетки становятся морфологически и цитохимически недифференцируемыми. Они характеризуются:
1. Изменением ядра и цитоплазмы (вместо крупных появляются клетки неправильной формы с увеличением площади ядра и цитоплазмы;
2. Обладают способностью расти вне органов гемопоэза (пролифераты из лейкозных клеток находят в коже, почках, головном мозге и в мозговых оболочках), они неравноценны и представляют разные этапы прогрессии;
3. Имеют скачкообразный уход опухоли из-под цитостатического воздействия, а также лучевого, гормонального;
4. Нарастание процесса в виде выхода бластных элементов в периферическую кровь, перехода от лейкопении к лейкоцитозу.
Этапы опухолевой прогрессии - это этапы злокачественности лейкоза. В основе данной прогрессии лежит нестабильность генетического аппарата лейкозных клеток, которым свойственен переход из неактивного состояния в активное. Раскрытие этапов лейкозного процесса имеет большое практическое значение, ибо главный его смысл заключается в поисках цитостатических препаратов, адекватных каждому этапу злокачественности.
Начиная разбор клинической картины лейкозов, необходимо коснуться вопроса о современной классификации заболевания, стадиях и диагностике.
Начиная с 1976 г. во всем мире клиницисты пользуются ФАБ (Франция, Америка, Британия) классификацией острых лейкозов. По которой лейкозы делятся на острый лимфобластный лейкоз /ALL/, 75-80% от всех лейкозов у детей, и острый нелимфобластный лейкоз ANLL, который включает в себя семь подтипов (М1 - М7) и составляет 20-25% лейкозов у детей.
М1,2 - острый миелобластный лейкоз, М 1 - недифференцируемая острая миелоидная лейкемия, М 2 - дифференцируемая миелоидная лейкемия, 15-18%, чаще у детей старшего возраста.
М 3 - острый промиелоцитарный лейкоз, 2-5%.
М 4 - острый миелобластный лейкоз, встречается очень редко.
М 5 - острая монобластная и моноцитарная лейкемия.
М 6 - острый эритромиелоз (эритролейкоз) - 1,25%.
М 7 - острая мегакариоцитарная лейкемия.
М 0 - острый недифференцируемый лейкоз.
Выживаемость при острых нелимфобластных лейкозах значительно ниже, чем при ОЛЛ. Однако в настоящее время она значительно возросла в связи с трансплантацией костного мозга от братьев или сестер, совместимых по HLA.
Для установления диагноза лейкоза необходимо цитологическое, цитохимическое и цитогенетическое исследование костного мозга и выявление поверхностных антигенных маркеров клеток (иммунофенотипирование L1, L2, L3).
С учетом морфологической характеристики ОЛЛ выделяют 3 подварианта (см. таблицу 4).
ТАБЛИЦА 4
Сравнительная цитологическая характеристика острого лимфобластного и острого миелобластного лейкоза у детей.
| Популяция |
Цитоплазма |
Ядро |
Ядрышки |
| АLL - L 1, малая, однороная,гомогенная популяция. |
Скудная с редкими вакуолями |
круглые, постоянно. |
0-1, от мелких до неопределенных. |
| АLL - L 2 от средних до больших; разнородная, гетерогенная популяция. |
от умеренной до большой; непостояннобазофильная с редкими вакуолями. |
от круглых до неправильных, уродливых. |
1, различимые или неразличимые. |
| ALL - L 3 от средних до больших. |
от умеренной до большой. |
от круглых до овальных. |
1 или больше, нечеткие. |
| AМL - М 1 от средних до больших. |
от средней до большой, палочки Ауэра |
от круглых до овальных, хроматин от тонкого до грубого. |
1 или больше, обычно различимые. |
ПРИМЕЧАНИЕ: М 1 - острая миелобластная лейкемия без зрелых форм.
ТАБЛИЦА 5.
Цитохимические реакции, характерные для острых лейкозов.
| АВ |
MP0 > 3 |
SBB > 3 |
CAE |
ANB |
PAS |
AP |
| L1 |
- |
- |
- |
-/+ |
+B |
-/+ |
| L2 |
- |
- |
- |
-/+ |
+A |
-/+ |
| L3 |
- |
- |
- |
-/+ |
- |
+ |
| M1 |
+ |
+ |
-/+ |
-/+ |
-/+ |
+/- |
| М2 |
+ |
+ |
+/- |
-/+ |
+ |
+/- |
| M3 |
+ |
+ |
+ |
-/+ |
+ |
+/- |
| M4 |
+ |
+ |
+/- |
+ |
+ |
+ |
| M5 |
-/+ |
-/+ |
-/+ |
+ |
+ |
+ |
MPO - миелопероксидаза
SBB - судан черный
PAS - периодическая Шифф - кислота (реакция на гликоген)
САЕ - хлорацетат эстераза
ANB - альфа нафтил бутиратэстераза
AP - кислая фосфатаза
Как видно из таблицы 5 L 1 и L 2 варианты ОЛЛ в большинстве PAS положительные, а L 3 вариант - отрицательный, в то время как нелимфобластные лейкозы дают положительную реакцию на миелопероксидазу и судан черный.
Для клинической практики выделение трех подвариантов ОЛЛ имеет очень большое значение, поскольку от подварианта зависит курс проводимой терапии и прогноз для жизни больного. Кроме того L 1 и L 2 подварианты могут быть Т-клеточной формой или ни-Т- ни В-клеточной формой, а L 3 подвариант В- клеточной формой.
При постановке диагноза ОЛЛ необходимо указать и стадию заболевания. В 1979 г. А.И. Воробьев и М.Д. Бриллиант предложили свою классификацию ОЛЛ. Согласно этой классификации выделяют начальный период, развернутую стадию болезни, полную ремиссию, выздоровление (состояние полной ремиссии на протяжении 5 лет), частичную ремиссию, рецидив с указанием, какой по счету, и уточнением очага локализации при локальном рецидиве, терминальная стадия.
Для прогноза заболевания имеет значение диагностирование на ранней стадии. Ни у кого нет сомнения сегодня, что ОЛЛ начинается постепенно и лишь его манифестация представляется острой. Многие исследователи пишут о "предлейкозе ", но в предлейкозе поставить диагноз нельзя. Поставить диагноз лейкоза позволяет морфологическая картина костного мозга с наличием 30% бластов и более. В начальном периоде ОЛЛ протекает под видом болезней, "масок ", связанных преимущественно с гиперпластическим поражением органов, либо с выраженным цитопеническим синдромом. Соответственно детям выставляется диагноз ревматизм, лимфаденит, инфекционный мононуклеоз, злокачественная лимфома и др., а с другой стороны апластическая анемия, геморрагический васкулит, тромбоцитопеническая пурпура, сепсис и др.
Следует подчеркнуть, что для раннего распознавания ОЛЛ у детей во всех неясных случаях о лейкозе надо думать чаще и прибегать к исследованию костного мозга. Особенно это имеет значение для постановки диагноза в алейкемическую стадию, когда в геммограмме еще отсутствуют бласты. К сожалению диагноз ОЛЛ чаще выставляется в лейкемическую стадию, при наличии бластов в геммограмме.
Пунктат костного мозга особенно необходимо исследовать в случаях, сопровождающихся цитопенией или увеличением лимфоузлов, либо тем и другим вместе, не применяя до этого никакого лечения (рентгеновское облучение, электрофорез, УВЧ, назначение преднизалона), так как такая терапия может ускорить течение лейкозного процесса и миелограмма будет нехарактерной, что затруднит постановку диагноза, оставит больного на долгое время без специфической терапии.
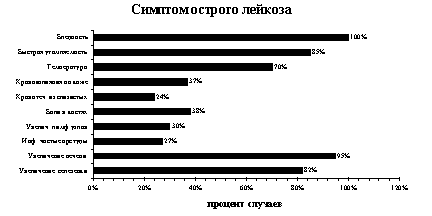
Для манифестных клинических проявлений ОЛЛ характерны увеличение лимфатических узлов, печени, селезенки, боли в костях и суставах, повышение температуры, бледность, быстрая утомляемость, недомогание, геморрагии. Реже появляется стоматит, головная боль, обмороки, изменения со стороны нервной системы.
В периферической крови находят либо алейкемическую картину, либо наличие бластных клеток, в костном мозге - 30% и более бластов. Если же диагноз острого лейкоза неубедителен (10-15% бластных клеток), то, возможно только симптоматическое лечение, необходимо повторно исследовать миелограмму через 3-4 недели.
В стадии полной ремиссии в пунктате костного мозга находят не более 5% бластных клеток, а общее количество бластных и лимфоидных клеток в нем не превышает 40%; в периферической крови бластных клеток не должно быть, в составе крови возможны умеренная лейкемия и тромбоцитопения, соответственно 3,0 * 109/л и 100,0 * 109/л из-за цитотоксического воздействия; должен быть нормальный состав спиномозговой жидкости и отсутствовать клинические признаки лейкозной пролиферации.
Частичная ремиссия может характеризоваться гематологическим улучшением, уменьшением бластных клеток в костном мозге, в спиномозговой жидкости при ликвидации клинических признаков нейролейкоза и (или) при подавлении очагов лейкозной инфильтрации в других органах, вне костного мозга.
Рецидив острого лейкоза бывает костномозговым (появление в пунктате более 5% бластных клеток) или внекостномозговым с различной локализацией лейкозной инфильтрации (нейролейкоз, лейкозная инфильтрация селезенки, лимфоузлов, гайморовых пазух, яичек и др.).
В терминальную стадию, клинически в значительной мере условную, вкладывается морфологическое понятие об исчерпании терапевтических резервов, о некурабельном этапе опухолевой прогрессии лейкоза. Вместе с этим отмечается условность этой стадии, поскольку она отражает лишь современный уровень терапевтических возможностей. Все цитостатические средства не только оказываются неэффективными, но и на их фоне прогрессирует лейкоз, нарастает цитопенический синдром, прежде всего агранулоцитоз, появляются некрозы на слизистых оболочках, сепсис, кровоизлияние. Терминальная стадия свидетельствует о необходимости отмены цитостатической терапии с сохранением симптоматической.
Причины смерти детей при лейкозах, в том числе лимфобластном, - это сепсис, кровоизлияния в мозг, интоксикация.
При остром лимфобластном лейкозе (ОЛЛ) выделяют прогностически неблагоприятные формы, которые влияют на выживаемость больного.
Особо выделяется нейролейкоз, который может присоединиться к любым локальным формам рецидива и стать самостоятельной формой, без проявления какой-либо другой клиники заболевания. В последние годы нейролейкоз стал частым проявлением рецидива заболевания. Это связывают с увеличением продолжительности жизни больных и с тем обстоятельством, что противолейкозные препараты не проникают через гематоэнцефалический барьер и для лейкозных клеток в центральной нервной системе создается определенное укрытие, благоприятные условия для проявления лейкозных инфильтратов.
НЕЙРОЛЕЙКОЗ (лейкозное поражение нервной системы) развивается вследствие метастазирования лейкознык клеток в оболочки головного и спинного мозга, в вещество мозга и нервные стволы. Диагноз нейролейкоза ставится на основании обнаружения бластных клеток в ликворе. При нейролейкозе в ликворе может наблюдаться вариобельный цитоз до нескольких тысяч клеток в 1 мкл., повышение уровня белка и снижение уровня глюкозы, цвет жидкости, как правило, сероватый, с положительной реакцией Панди.
Клинических проявлений при нейролейкозе, кроме обнаружения цитоза в ликворе, может и не наблюдаться; в то же время они могут быть самыми разнообразными. Это изменение поведения ребенка: раздражительность, вялость, необщительность. Появляется головная боль, тошнота, рвота (при менингиальной форме), очаговая симптоматика в виде поражения черепных нервов, пирамидной недостаточности, мозжечковых симптомов, судорог, нарушения речи и сознания (при менингоэнцефалической и энцефалической форме ), нижних парапарезов, нарушение походки и функции тазовых органов, корешковых симптомов (при менингомиелитической форме). Экзофтальм наблюдается, как правило, при хлорлейкозе.
Почти у половины больных при рецидиве лейкоза отмечается нормальный состав периферической крови, и поэтому большое значение имеет внимательный осмотр больного, своевременная костно-мозговая и люмбальная пункции при диспансерном наблюдении.
ТАБЛИЦА 6.
Прогностические признаки при ОЛЛ у детей (по Л.А. Махоновой и др., 1986г.).
| Фактор прогноза |
Благоприятный |
Неблагоприятный |
| Период от начала болезни до постановки диагноза. |
< 3 мес. |
> 3 мес. |
| Возраст больного. |
2 - 10 лет. |
До 2 лет и свыше 10 лет. |
| Увеличение периферических лимфоузлов. |
< 2 см. |
> 2 см. |
| Увеличение печени. |
< 4 см. |
> 4 см. |
| Увеличение селезенки. |
< 4 см. |
> 4 см. |
| Поражение ЦНС. |
Нет. |
Есть. |
| Лейкоцитоз. |
До 20,0 * 109/л |
Свыше 20,0 *109/л |
| Гемоглобин. |
< 70 г/л |
> 70 г/л |
| Тромбоциты. |
< 100,0 * 109/л |
> 100,0 * 109/л |
| Иммуноглобулины. |
Норма |
Снижены |
| Морфология бластов по ФАБ - классификации. |
L 1 |
L 2, L 3 |
| Иммунология бластов. |
Т-клетки |
В-клеточная |
| Цитохимические данные: кислая фосфотаза |
Отрицательная |
Положительная |
| ШИК-реакция. |
Положительная |
Отрицательная |
Клинические маски острого лейкоза самые разнообразные: лимфаденит, эпид, паротит, туберкулез, лимфогранулематоз, ревматизм, ревматоидный артрит, гепатиты, инфекционный мононуклеоз, острый аппендицит, затяжные простудные заболеванияы, длительные язвено - некротические стоматиты, ангины, сепсис, апластическая анемия, гемолитическая анемия, тромбоцитопеническая пурпура, геморрагический васкулит, дизентерия, мелкоочаговая пневмония.
 |
|
рис. 2. |
|
|
|
рис. 3. |
Лейкопения - ниже 4*109
Тромбоцитопения - ниже 100*109
ЛЕЧЕНИЕ ОСТРОГО ЛИМФОБЛАСТНОГО ЛЕЙКОЗА.
С 1990 года в гематологическом отделении Республиканской клинической детской больницы применяют современные терапевтические протоколы лечения острого лимфобластного лейкоза у детей ОЛЛ-БФМ-90 разработанные немецкими коллегами (1988, 1990, 1992гг.). По протоколам среди детей, больных ОЛЛ, выделяют три группы риска:
1. Группа стандартного риска - дети от 1 года до 6 лет. Количество бластов на 8 день терапии в периферической крови не превышает 1000 в 1 мкл. (после 7-дневного приема преднизалона); отсутствует пре-Т иммунофенотип лейкоза (если у пациента не проводилось иммуноспецифическое исследование бластов, но имеется медиастенальная опухоль, то пациент в любом случае из стандартной группы риска); не имеется первичного поражения ЦНС; установлена полная ремиссия на 33 -й день лечения;
2. Группа среднего риска - дети до 1 года и старше 6 лет, количество бластов в периферической крови на 8 -й день, после 7-дневной преднизолоновой профазы, не превышает 1000 в 1 мкл; полная ремиссия на 33 -й день лечения;
3. Группа высокого риска - отсутствие полной ремиссии на 33 -й день лечений.
Между 65 и 70 днем повторная контрольная костномозговая пункция для подтверждения ремиссии, если на 33 день в костном мозге 5% и более бластов
(в гемограмме не более 20 х 109 /л лейкоцитов).
КЛАССИФИКАЦИЯ ЦИТОСТАТИЧЕСКИХ СРЕДСТВ.
Противолейкозные препараты.
1 Антиметаболиты - нарушают синтез предшественников нуклеиновых кислот, путем конкуренции с последними в лейкозной клетке.
Метотрексат - антогонист фолиевой кислоты (эффект в стадии разгара и в качестве поддерживающей терапии, действует на S фазу).
Ланвис (Tioguaninum) ( Glaxo Wellcome) - 1 табл. содержит 40 мг тиогуанина : 25 табл. в упаковке. Тиогуанин является сульфгидрильным аналогом гуанина и проявляет свойства пуринового антиметаболита. Являясь структурными аналогами пуриновых нуклеотидов, метаболиты тиогуонина включаются в пуриновый обмен и ингибируют синтез нуклеиновых кислот в опухолевых клетках.
6-Меркаптопурин (пуринетол) - антогонист пурина, вмешивается в обмен нуклеиновых кислот, действует на S фазу.
Цитозар (цитозинарабинозид) - систематический аналог пиримидина, препятствует превращению цитидина в диоксицитидин (на S фазу лейк. клетки).
2 Алкилирующие соединения - подавляют синтез ДНК и в меньшей степени РНК в лейкозной клетке.
циклофосфан, обладающий цитостатическим и цитолитическим действием на лейкозные клетки.
3 Алколоиды растений.
Винкристин - практически воздействует на все фазы покоящейся клетки.
Этопозид (вепезид, VP -16) - из растений мондрагоры, предотвращает вхождение клетки в митоз.
4 Ферментные препараты.
L-аспарагиназа (краснитин) - разлагает аспарагин, необходимый для синтеза протеина, на аспарагиновую кислоту и амоний в лейкозной клетке, которая не способна к самостоятельному синтезу аспарагина и поэтому погибает от его эндогенного действия.
5 Противоопухолевые антибиотики.
Адриамицин, рубомицин - обладает цитостатическим действием, подавляет синтез нуклеиновых кислот путем взаимодействия с ДНК и РНК - полимеразами.
6 Гормональные препараты.
Преднизолон - обладает цитолитическим действием на лейкозные клетки (лимфобласты и недифференцируемые бласты) и не вызывает разрушения нормальных лимфоцитов.
ТЕРАПЕВТИЧЕСКИЕ ПРОТОКОЛЫ.
Дозировка медикаментов осуществляется в соответствии с площадью поверхности тела пациента. Каждый раз перед началом нового этапа лечения вновь определяется площадь поверхности тела и расчитывается соответственно доза препаратов. При эндолюмбальной инъекции и при облучении головы дозировка осуществляется в соответствии с возрастом.
Полихимиотерапия больных со стандартным и средним факторами риска длится в течение 6-ти месяцев.
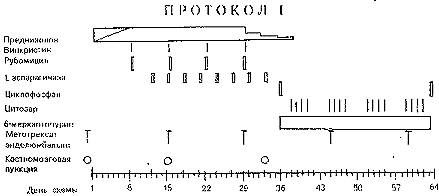
ПРОТОКОЛ I - (направлен на редукцию ремиссии), см. рис.4.
 |
|
Рис. 4 |
Первая фаза. Преднизолон назначается из расчета 60 мг/м2 с 1-го по 28 день, затем снижение дозы на 50% каждые три дня до полной отмены. У пациента с высокой начальной массой лейкозных клеток или выраженной органомегалией начальную дозу необходимо назначать из расчета 20 мг/м2, до снижения уровня лейкоцитов в периферической крови ниже 20 * 109/л, чтобы избежать острого синдрома распада белков.
В зависимости от клинического ответа на терапию (уменьшение органов), лабораторных показателей (уменьшение числа лейкоцитов, содержания мочевой кислоты, мочевины, креатинина, калия) дозу преднизалона нужно быстро увеличивать до окончательной (60 мг/м2) не позднее 5-го дня терапии.
Винкристин вводится в дозе 1,5 мг/м2 внутривенно на 8, 15, 22, 29-й день.
Рубомицин вводится из расчета 30 мг/м2 внутривенно капельно в течении 1 часа на 8, 15, 22, 29-й день. Перед первым введением рубомицина делается ЭКГ и эхография сердца (препарат кардиотоксичен).
L-Аспариназа (L-ASP) - вводится в дозе 10000 ед/м2 внутривенно капельно в течении 1 часа на 8, 15, 18, 21, 24, 30, 33-й день.
Возможны тяжелые аллергические реакции, гипергликемия и нарушение свертывания крови. Необходимо проводить лабораторный контроль свертывания крови (фибриноген, АТ-Ш, плазминоген), уровня сахара. При развитии анафилаксии возможна замена на эрвиназу.
Профилактика нейролейкоза проводится эндолюмбальными введениями метотрексата в возрастной дозировке 1 раз в 2 недели.
Вторая фаза. Условия для начала фазы 2 протокола 1 следующие: полная ремиссия в костном мозге, менее 5% бластов в миелограмме; при начальном поражении ЦНС - полная ремиссия в ЦНС; при медиастенальной опухоли - уменьшение размеров опухоли до 30% ее начальной величины; удовлетворительное общее состояние; отсутствие тяжелой инфекции; креатинин в пределах возрастной нормы; лейкоциты более 2 * 109/л; гранулоциты - более 0,5 * 109/л.
Циклофосфан (ЦФ) - вводится в дозе 1000 мг/м2 внутривенно капельно в течении часа на 36-й и 64-й день лечения. Контроль диуреза и профилактика геморрагического цистита проводятся следующим образом: гидратация 3000 мл/м2 за 24 часа; фуросемид из расчета 0,5 мг/кг внутривенно на 6 и 12 час после циклофосфана; месна (урометоксан) 400мг/м2 внутривенно на 0,4 и 8 часу от начала инфузии циклофосфана.
6-Меркаптопурин (6-МП) - 60 мг/м2 в сутки внутрь, 36- 63-й дни лечения.
Цитозар (ARA-C) - 75 мг/м2 в сутки внутривенно в виде 4 дневных блоков; 38-41 дни, 45-48, 52-55, 59-62 дни. После начала лечения цитозаровые блоки желательно не прерывать. Если начало цитозаровых блоков откладывается или прерывается, одновременно прекращается прием 6-МП. Выпавшее в лечении 6-МП нужно подтянуть до общей плановой кумулятивной дозы, равной 1680 мг/м2.
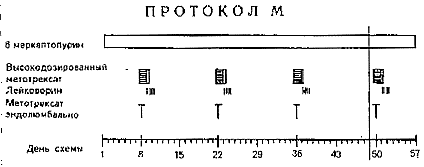
ПРОТОКОЛ М - ( направлен на консолидацию ремиссии), см. рис.5.
 |
|
Рис. 5 |
включает в себя 6-меркаптопурин, высокодозированный метотрексат, метотрексат эндолюмбально, лейковорин внутривенно. Начинается через 2 недели после завершения протокола 1. Основные условия для начала этого протокола: лейкоциты больше 1,5 * 109/л; гранулоциты больше 0,5 * 109/л; тромбоциты больше 50 * 109/л.
6-Меркаптопурин назначается из расчета 25 мг/м2 в день (внутрь), в течение 8 недель.
Метотрексат назначается в дозе 1 г/м2 ( 1/10 общей дозы, вводится в течение 30 мин; 9/10 общей дозы вводится в течение 35,5 ч.) путем непрерывной инфузии, на 8, 22, 36, 50 день от начала протокола М.
Лейковорин (антидот метотрексата) дается из расчета 15 мг/м2 внутривенно струйно или внутрь в таблетках на 42, 48, 54 час от начала введения.
МТХ интралюмбально вводится через 2 часа от начала внутривенной инфузии МТХ в возрастной дозировке.
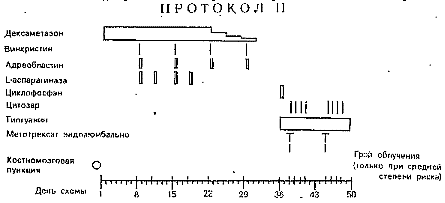
ПРОТОКОЛ II - (также направлен на консолидацию ремиссии), см. рис.6.
 |
|
Рис.6 |
Первая фаза. Проводится через две недели после протокола М. Условия начала П протокола следующие: продолжается полная ремиссия; хорошее общее состояние больного; отсутствие инфекции; лейкоциты больше 2,5* 109/л; гранулоциты больше 1*109/л; тромбоциты больше 100 * 109/л.
Дексаметазон 10 мг/м2 внутрь с 1 по 21 день от начала протокола, затем дозу уменьшают каждые 3 дня на 50% до полной отмены.
Винкристин 1,5 мг/м2 - 4 внутривенных введения с интервалом в одну неделю (максимальная доза 2 мг/м2).
Адриамицин (ADR) 30 мг/м2, инфузия в течение 1 часа. Перед 1 и 3 назначением необходимо провести ЭКГ и эхокардиографическое исследование: при признаках снижения сократительной функции миокарда следует прекратить дальнейшее применение ADR.
L-Аспарагиназа 10000 ЕД/м2 - инфузия в течение 1 часа на 8, 11, 15, 18 день.
Вторая фаза. Условия для начала второй фазы протокола П: хорошее общее состояние; отсутствие инфекций; нормальный возрастной уровень креатинина в сыворотке крови; лейкоциты больше 2 * 109/л; гранулоциты больше 0,5 * 109; тромбоциты больше 50 * 109/л.
Циклофосфан 100 мг/м2, инфузия в течение 1 часа на 36 день от начала протокола. Контроль диуреза и профилактика цистита такие же, как в протоколе 1.
6-Тиогуанин (6-TG) 60 мг/м2 внутрь в 36-49 дни, всего 14 дней.
Цитозар (ARA-C) 75 мг/м2 внутривенно двумя блоками через 4 дня: 38-41 день, 45-48 дни.
МТХ интралюмбально вводится в возрастных дозировках на 38 и 45 день от начала протокола.
Облучение головы. При хорошем клиническом состоянии облучение головы начинается с 38 дня протокола П для детей из групп среднего и высокого риска. Доза облучения зависит от возраста и от начального вовлечения ЦНС (от 12 до 18 Гр детям до 2 лет, от 18 до 24 Гр детям старше 2 лет).
В случае выявления нейролейкоза люмбальные пункции метотрексата осуществляются один раз в неделю, с одновременным введением цитозара, преднизолона. В конце полихимиотерапии подключается облучение головы.
Поддерживающая терапия проводится двумя препаратами сроком до 2-х лет .
6-Меркаптопурин 50 мг/м2 внутрь, ежедневно.
Метотрексат 20 мг/м2 внутрь 1 раз в неделю. В день приема необходимо контролировать общий анализ крови и регулировать дозу поддерживающей терапии в зависимости от уровня лейкоцитов (при уровне лейкоцитов 1-2 * 109/л - 50% доза 6 МП/МТХ, 2-3 * 109/л - 100%, более 3 * 109/л - 150 %).
В республиканской детской больнице выживаемость детей с ОЛЛ была около 10-12%. 1990 г., после начала работы по протоколам БФМ выживаемость детей с первичным ОЛЛ составила 90%, ремиссия 95%, 5 -летняя выживаемость 69%.
После изложения основной терапии по протоколам БМФ - 90 необходимо остановиться на клиническом патоморфозе лейкозов.
Само понятие "патоморфоз" (греч.) - стойкое изменение количественных и качественных сдвигов нозологии под влиянием в данном случае лечения: стойкое изменение лимфобластных лейкозов.
К проявлениям патоморфоза относится поражение органов лейкозным процессом с присущими ему интоксикацией, инфильтрацией, кровоизлияниями и анемической гипоксией, а также побочным действием цитостатиков. В процессе лечения с наступлением ремисси редуцируется лейкозная опухоль и уходят ее проявления в органах и системах, но сохраняются побочные действия цитостатиков, ибо после наступления ремиссии продолжается специфическая химио- и лучевая терапия .
Самым важным звеном в этом патоморфозе является цитопенический синдром, когда разрушены бласты и нормальное кроветворение еще не восстановилось. В этом опустошении без кроветворных клеток организм подстеригает череда осложнений: синдром разрушения бластов (знаменитая тетрада - гиперурекимия, гиперкалиемия, гиперфосфатемия, гипокальциемия), ДВС-синдром, сепсис и кровоизлияния, поражение сердца, печени, кишечника и др. органов. В этот период даже при отсрочивании назначений цитостатиков, действие их на организм еще продолжается. Все это создает сложную ситуацию, в которой необходимо предусмотреть помощь всему организму в целом, поэтому большое значение при лечении ОЛЛ имеет, так называемая, сопроводительная терапия.
С целью противодействия синдрому лизиса опухоли, с первых дней лечения проводится массивная инфузионная терапия (3000 мл/кв.м в сутки) глюкозо-солевыми растворами. Для профилактики и лечения инфекционных осложнений широко используются противовирусные препараты Зовиракс (ацикловир), Вальтрекс Glaxo Wellcome и др., антибиотики цефалоспорины П-го поколения (Зинацеф, Glaxo Wellcome) и Ш-го поколения (Фортум, Glaxo Wellcome,Роцефин, F.Hoffmann-La Roche и др.), аминогликозиды и др., антиникотические средства - дифлюкан, амфотерицин.
Адекватным антиперетиком является парацетамол (Gllaxo Wellcome). Одним из наиболее эффективных антиэметических препаратов является Зофран (Glaxo Wellcome). Арсенал препаратов, используемых в качестве сопроводительной терапии при ОЛЛ у детей очень велик.
|